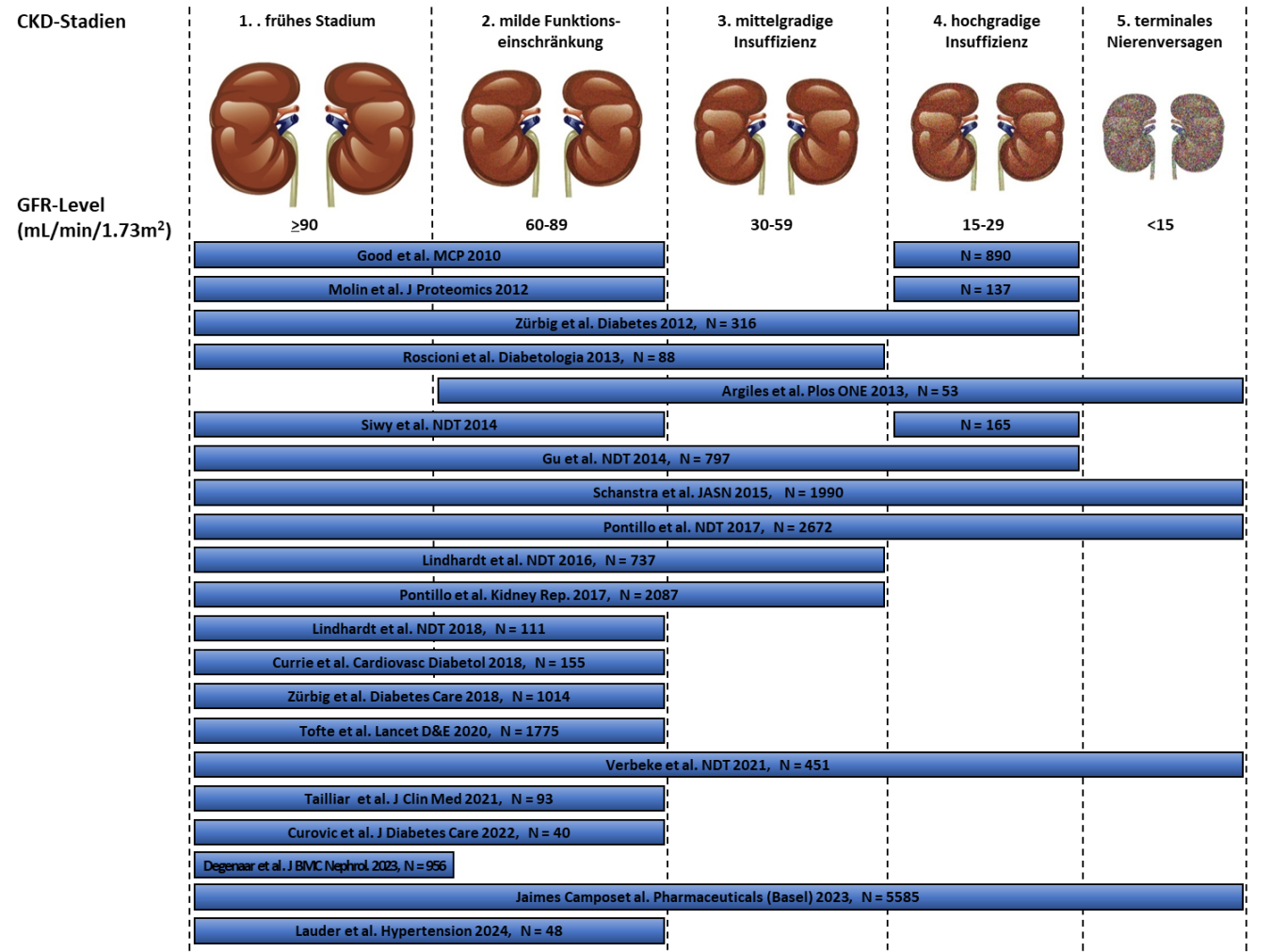
Einsatz des CKD273-Tests in vielen Studien. Modifiziert nach Critselis et al. [2].
Frühe Erkennung
Moderne, nicht-invasive diagnostische und prognostische Verfahren stehen heute zur Verfügung und ermöglichen eine zuverlässige Diagnose, Prognoseeinschätzung sowie eine gezielte Auswahl von Therapien.
Patienten mit relevanten Risikofaktoren (Diabetes, Hypertonie, Alter, Übergewicht, möglicherweise eingeschränkte Nierenfunktion, nicht näher spezifizierte Auffälligkeiten im Urin) für eine Nierenerkrankung sollten daher eine molekulare Diagnostik in Betracht gezogen werden.
Eine in vielen Studien erprobte nicht-invasive Methode zur Früherkennung oder zum Ausschluss einer chronischen Nierenerkrankung (CKD) ist das Urinproteommuster CKD273, basierend auf einem AI-Algorithmus, der 273 Peptide und Proteine im Urin beurteilt [1]. Dieses Proteommuster wurde bereits 2016 von der US-FDA akzeptiert und mit dem "Letter-of-Support" bedacht.
Wird CKD mit diesem Urintest bestätigt, kann die Differentialdiagnose mittels Proteomanalyse zwischen verschiedenen chronischen Nierenerkrankungen unterscheiden.
Referenzen:
[1] Good DM et al, Mol Cell Proteomics. 2010, 9(11):2424-37.
[2] Critselis E et al, Nephrol Dial Transplant. 2016, 31(2):249-54.
Liquid Biopsie mittels Proteomanalyse
Bestimmte relevante Erkrankungen können anhand der Krankengeschichte, bildgebender Verfahren und des Vorliegens von Diabetes ausgeschlossen oder bestätigt werden [3].
Eine akute Nierenschädigung (AKI), die durch Kreislaufprobleme verursacht wurde, kann meist sicher anhand der Krankengeschichte diagnostiziert werden. Charakteristische Bildgebungsmerkmale ermöglichen zudem die Diagnose einer autosomal-dominanter polyzystischer Nierenerkrankung (ADPKD), sowie von obstruktiven Nierenerkrankungen, wie angeborenen Fehlbildungen des Urogenitaltrakts (CAKUT).
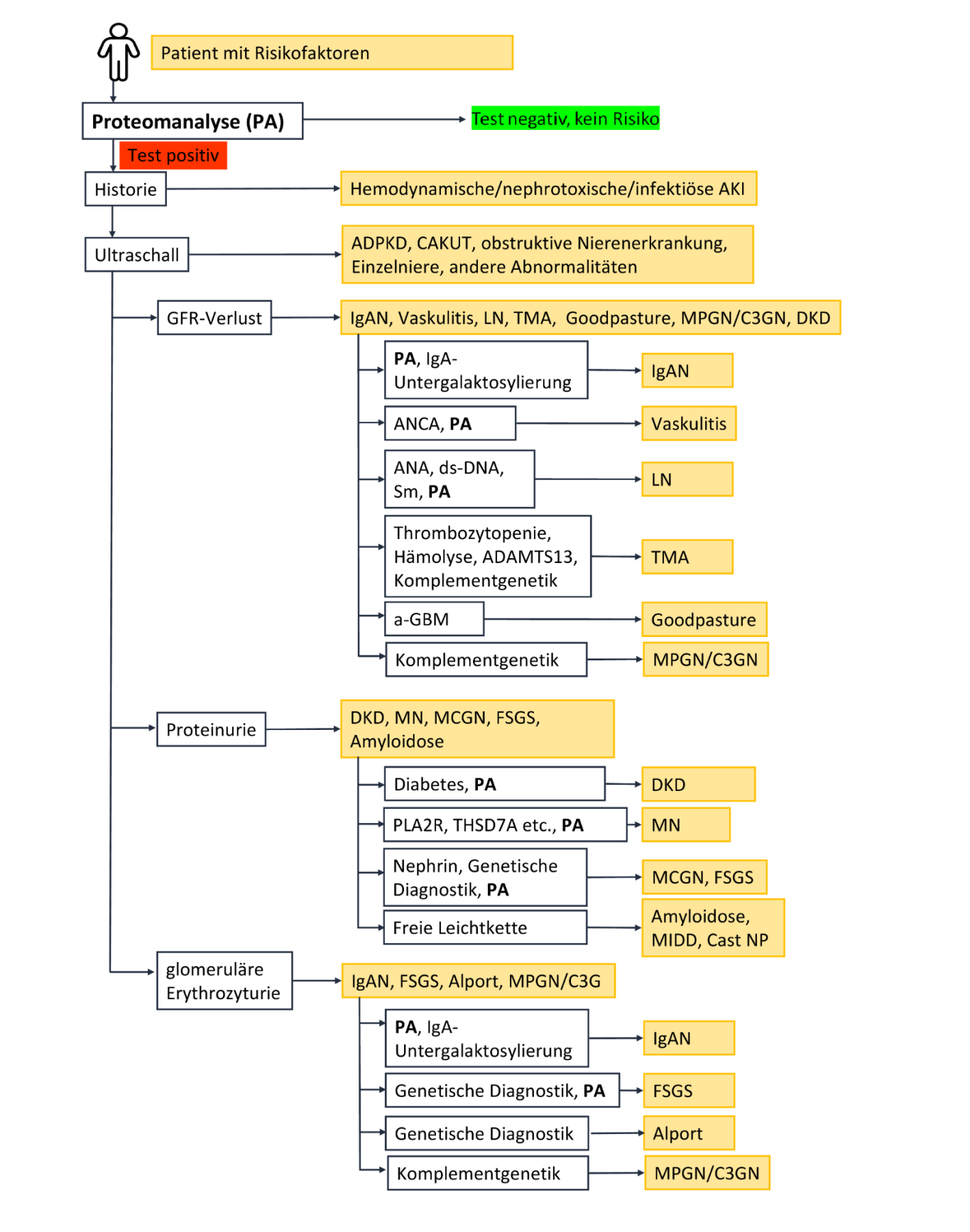
Bei strukturellen Nierenerkrankungen, die nicht durch Diabetes oder Hypertonie verursacht werden, ist der nächste diagnostische Schritt die differential-diagnostische Bestimmung der Erkrankung. Dazu kann die Proteomanalyse (PA) [4, 5] eingesetzt werden. Bei glomerulärer, nephrotischer und nicht-selektiver Proteinurie sollte an membrano-proliferative Glomerulonephritis (MPGN/C3GP), fokal-segmentale Glomerulosklerose (FSGS), Minimal-Change-Glomerulonephritis (MCGN), membranöse Nephropathie (MN) oder Nierenamyloidose gedacht werden. Nierenamyloidose kann durch das Verhältnis von Lambda- und Kappa-Leichtketten bestätigt oder ausgeschlossen werden. Membranöse Nephropathie (MN) ist anhand spezifischer Autoantikörper nachweisbar. Falls weder ein auffälliges Leichtketten-Profil noch Autoantikörper für MN vorliegen, sind MCGN oder FSGS wahrscheinlich. Des Weiteren gibt es noch die Möglichkeit, eine primäre von einer sekundären FSGS mittels der Proteomanalyse zu unterscheiden [6].
Entzündliche Glomerulopathien sind durch die Ausscheidung von Erythrozyten im Urin gekennzeichnet. Eine weitergehende Differenzierung ist durch hochspezifische Urin-Proteommuster oder genomische Analysen möglich. Das Alport-Syndrom kann anhand dysmorpher Erythrozyten im Urin sowie durch bekannte Mutationen im Kollagen-IV-Gen diagnostiziert werden. Die IgA-Nephropathie (IgAN), die weltweit häufigste Glomerulonephritis, kann mit hoher Treffsicherheit durch das Urinproteommuster IgAN237 nachgewiesen werden [7].
Ein rascher Funktionsverlust der Niere, kombiniert mit Proteinurie und dysmorphen Erythrozyten im Urin, spricht für eine Erkrankung des gesamten glomerulären Kompartiments mit extrakapillärer Proliferation. Das Goodpasture-Syndrom kann durch den Nachweis von Antikörpern gegen die glomeruläre Basalmembran diagnostiziert werden. Bei autoimmuner Vaskulitis sind ANCA-Antikörper wegweisend. Lupus-Nephritis kann durch den Nachweis von antinukleären und dsDNA-Antikörpern diagnostiziert werden.
Dank jahrzehntelanger Forschung ist es heute möglich, die diagnostische Zuverlässigkeit von Biomarkern, genetischen Analysen und Proteommustern anhand der bisherigen histomorphologischen Goldstandards zu bewerten. Die ersten Schritte hin zu einer nicht-invasiven „Liquid-Biopsie“ sind bereits gemacht. Diese Technologie kann heute schon angewendet werden und eine Nierenbiopsie mit ihren Risiken vermeiden.
Referenzen:
[3] Catanese L et al, Int J Mol Sci. 2024, 25(6):3519.
[4] Siwy J et al, Nephrol Dial Transplant. 2017, 32(12):2079-2089.
[5] Mavrogeorgis E et al, Nephrol Dial Transplant. 2024, 39(3):453-462.
[6] Catanese L et al, Clin Kidney J. 2023, 17(2):sfad296.
[7] Rudnicki M et al, Nephrol Dial Transplant. 2021, 37(1):42-52.
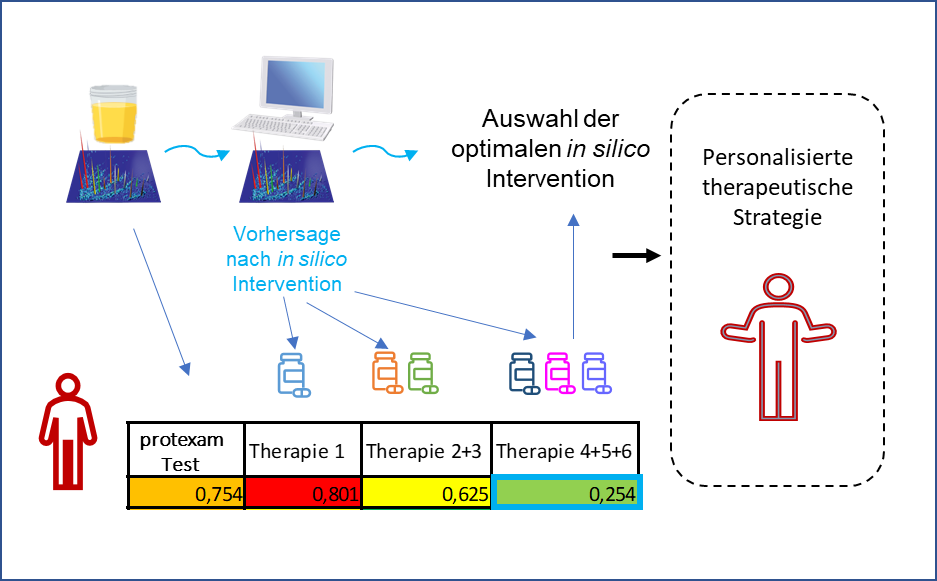
Vorschlag einer optimalen Therapie
Auf Grundlage des Proteommusters im Urin kann im Weiteren auch vorhergesagt werden, auf welche Medikamente oder andere therapeutische Interventionen (z.B. Änderungen des Lebensstils, Ernährung, etc.) die/der Patient/in ansprechen wird. Auf diese Art kann die optimale, personalisierte Therapie in-silico für jeden Patienten ermittelt werden [8, 9].
Referenzen:
[8] Jaimes Campos MA et al, Pharmaceuticals (Basel). 2023, 16(9):1298.
[9] Latosinska A et al, J Transl Med. 2025, 23(1):943.
